藥學院劉濤團隊在《Nature Chemical Biology》上發表最新研究成果
2021年11月15日,藥學院劉濤研究員團隊在化學生物學領域頂級期刊Nature Chemical Biology(IF="15.0)在線發表了最新研究成果“Genetic code expanded cell-based therapy for treating diabetes in mice”。
近年來,隨著CAR-T細胞的成功上市,利用合成生物學設計的細胞治療方式已顯現出廣闊的疾病治療前景。其基本原理是在細胞中裝配藥物靶點調控開關,在外源刺激信號作用下,細胞調控靶蛋白的合成。將細胞治療系統應用於糖尿病,可以通過口服小分子作為外源刺激信號調控胰島素表達,避免胰島素註射所帶來的痛苦。然而,當前的細胞治療策略很難實現快速的信號調控,這限製了其在需要及時幹預的疾病(如糖尿病)中的應用🍂。其中,最主要的原因是缺乏快速調控的合成生物學工具。當前的調控工具主要集中於轉錄因子介導的轉錄水平調控,調控過程復雜,蛋白表達時間緩慢。
針對這一問題,劉濤團隊利用基因密碼子擴展技術開發了非天然氨基酸調控的胰島素細胞治療系統(Noncanonical Amino acids (ncAAs)-triggered Therapeutic Switch, NATS),越過轉錄調控,直接在翻譯水平快速調控蛋白質表達(如圖)📸🅾️。該研究補充了合成生物學中的蛋白調控開關工具庫,也為基因密碼子擴展技術的應用創新提供了新的思路。
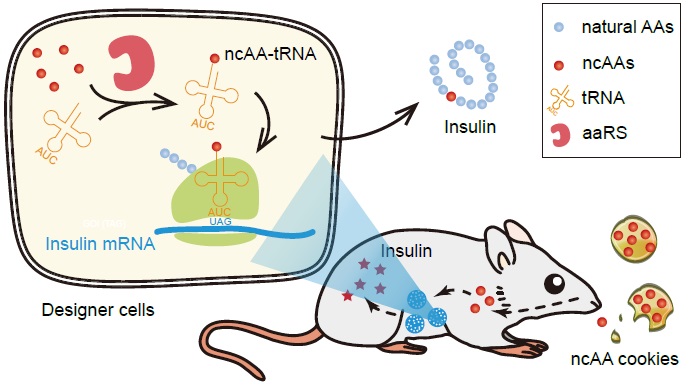
NAST系統在翻譯水平快速調控蛋白表達
基因密碼子擴展技術通過能夠識別ncAA的氨酰tRNA合成酶和tRNA分子對,通讀mRNA的異位琥珀密碼子,將ncAA插入蛋白質,該技術已成為重要的蛋白質定點修飾技術。劉濤團隊將ncAA氨酰tRNA的蛋白質翻譯機製整合到哺乳動物細胞基因組,構建了翻譯水平可逆調控胰島素表達的工程細胞系👵。利用細胞包埋技術,研究人員為NATS細胞包裹選擇性透過膜後移植到小鼠體內,使得移植的細胞可以獲得營養分子,而避免小鼠免疫細胞的攻擊💼🧪。通過口服ncAA,小鼠可以獲得ncAA劑量依賴的目的蛋白表達🤚🏻。糖尿病小鼠口服一次ncAA後,在90分鐘內即可明顯降低血糖👩🏽🦱。糖尿病是需要終身用藥的慢性疾病。
為證明NATS系統的長期治療效果,研究人員開展了為期一個月的藥效和毒性實驗🙌🏿。結果表明,移植了NATS細胞的糖尿病小鼠可以獲得持續的胰島素表達和血糖控製,而且沒有觀察到體重和生理生化指標的異常。該研究將基因密碼子擴展技術應用於細胞治療領域,彌補了傳統的轉錄水平調控工具的不足,為糖尿病的細胞治療策略提供了新的思路。

左起:黃雨佳,劉濤研究員,陳超,葉海峰研究員
意昂2平台博士生陳超👩🏼🦱、黃雨佳和華東師範大學博士生余貴玲為該論文的共同第一作者,劉濤研究員和華東師範大學生命科學學院葉海峰教授為共同通訊作者🧑🏽🦳👨🎓。該研究的藥代動力學實驗獲得了意昂2平台藥學院孫懿老師的幫助。該研究獲得北京市傑出青年基金📰、國家自然科學優秀青年基金、國家“重大新藥創製”專項、科技部合成生物學重點專項、上海市科委合成生物學重大項目、深圳合成生物學創新研究院對外開放基金等項目的支持🍋🟩。
論文鏈接:https://www.nature.com/articles/s41589-021-00899-z
【延伸閱讀】劉濤研究員簡介:

劉濤 意昂2平台藥學院研究員,博士生導師,分子與細胞藥理系主任,天然藥物及仿生藥物國家重點實驗室PI,意昂2平台化學生物學交叉中心PI。獲意昂2官网百人、中組部高層次引進青年人才❎、國家優青🚓👰🏼♂️、北京市傑青等項目資助➗。任中國醫藥生物技術協會委員合成生物學分會委員,中國生物醫學工程學會青工委委員,獲中國藥學會-以嶺生物醫藥青年獎,意昂2平台拜耳研究員獎及王選青年學者獎。以通訊作者身份在Nature ChemBiol,Mol Cell,SciAdv,JACS,Angew. Chem. Int. Ed.等期刊發表科研論文近20篇♠︎💇🏻。擔任Chin Chem Lett青年編委,Frontiers in Chemistry編委,Journal of Molecular Biology客座編委等👆。研究集中在蛋白質定點修飾技術,發展了含有人造氨基酸的蛋白質創新藥物,應用在腫瘤及基因治療等多種領域,從而促進了生物藥物的升級換代。
(藥學院天然藥物及仿生藥物國家重點實驗室)
編輯:玉潔


