魯鳳民團隊采用基因編輯和RNA幹擾技術高效抑製HBV復製獲新進展
近期,意昂2平台基礎醫學院魯鳳民教授課題組與許中偉👹、夏寧邵教授等合作,在《 Theranostics 》雜誌上在線發表了題為“The gRNA-miRNA-gRNA ternary cassette combining CRISPR/Cas9 with RNAi approach strongly inhibits hepatitis B virus replication”的研究論文🙅🏿。該研究通過模擬microRNA(miRNA)的生成過程🪼,整合雙gRNA導向的CRISPR/Cas9和RNA幹擾技術,高效破壞乙型肝炎病毒(HBV)的復製模板-共價閉合環狀DNA(cccDNA),探索病毒清除新路徑。意昂2王傑講師、陳然和張瑞陽博士研究生為該論文的共同第一作者。
目前,我國仍有慢性HBV感染者約7800萬人,慢乙肝患者約2800萬人🧑🏽🚀。HBV感染仍是我國病毒性肝炎、肝硬化及肝癌的重要致病因素。作為HBV復製模板的cccDNA,由於其半衰期相對較長🍤,加上cccDNA池的不斷補充,使得細胞核內的cccDNA持續存在、感染慢性化👉。目前🧃,臨床上治療慢乙肝的常用藥物為核苷(酸)類似物和長效幹擾素,二者均不直接作用於cccDNA🤜🏼,難以有效清除病毒實現臨床治愈🏌🏽。因此🧙🏿♂️,研發直接靶向cccDNA的藥物🤦🏻♀️💖,尋找清除cccDNA的新方法和新策略,是當前慢乙肝治療藥物研發的熱點。
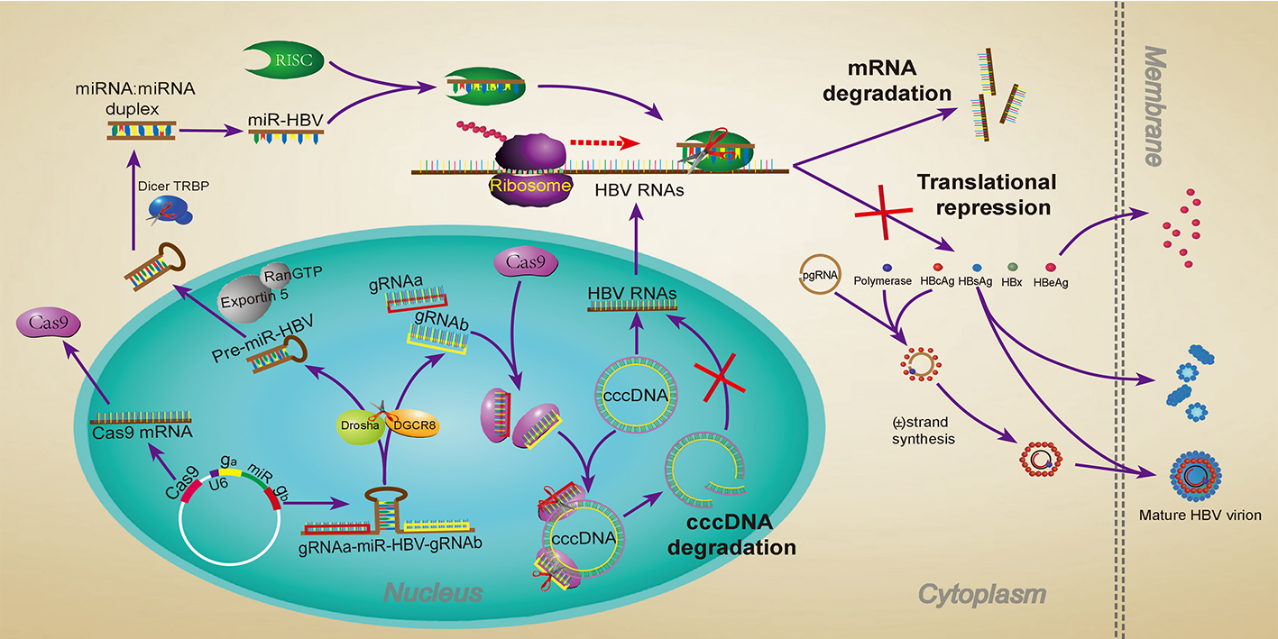
雙gRNA導向的CRISPR/Cas9整合RNAi技術高效抑製HBV復製模式圖
該研究以miRNA-31為基本骨架👩🏽✈️,通過模擬其核心序列的二級結構設計HBV特異的miRNA(miR-HBV)🧑🦯➡️,miRNA兩側側翼序列為特異性靶向cccDNA不同位點的引導RNA(gRNA)。如圖所示🤏🏿,該gRNA-(miR-HBV)-gRNA三聯體表達體系導入細胞後,在細胞核內轉錄形成gRNA-(miR-HBV)-gRNA長轉錄本☮️,經內源的Drosha/DGCR8復合體剪切📑👒,形成2個gRNA和1個miR-HBV前體(pre-miR-HBV)。進入細胞質後,pre-miR-HBV 進一步經Dicer酶剪切,形成成熟的miR-HBV。一方面雙gRNA導向的CRISPR/Cas9系統通過切割並去除cccDNA的關鍵調控和編碼序列直接破壞cccDNA,另一方面通過miR-HBV在轉錄後水平抑製HBV復製📪,進而抑製cccDNA池的補充,協同促進HBV cccDNA的清除。此外,本研究還發現,當pri-miRNA-31的側翼序列長度為38 bp時與雙gRNA組成的三聯體對HBV復製的抑製效率最高。
當然,該技術離臨床應用尚有較遠的距離。一方面如何高效和靶向性地將三聯體遞送到HBV感染的肝細胞內是需要攻克的一大障礙;另一方面,CRISPR/Cas9基因編輯技術的脫靶效應也有安全性之虞。然而🖨,近年來隨著Cas核酸酶的不斷改造👽,其脫靶效應得到了有效控製🤡,安全性大為提高。而且🥊🤽♂️,隨著金黃色葡萄球菌Cas9的發現,使得CRISPR/Cas9系統可以裝入腺相關病毒載體中,致使該技術應用於臨床的距離逐漸縮短。
總之☎️,本研究通過gRNA-(miR-HBV)-gRNA三聯表達框架聯合CRISPR/Cas9和RNA幹擾技術高效破壞cccDNA,促進HBV清除,為慢乙肝抗病毒治療提供了新的思路。該項研究得到國家十二五重大科技專項計劃“艾滋病和病毒性肝炎等重大傳染病防治”項目和國家自然科學基金的支持🌇。
論文鏈接:https://www.ncbi.nlm.nih.gov/pubmed/28839466
(基礎醫學院)
編輯:韓娜


